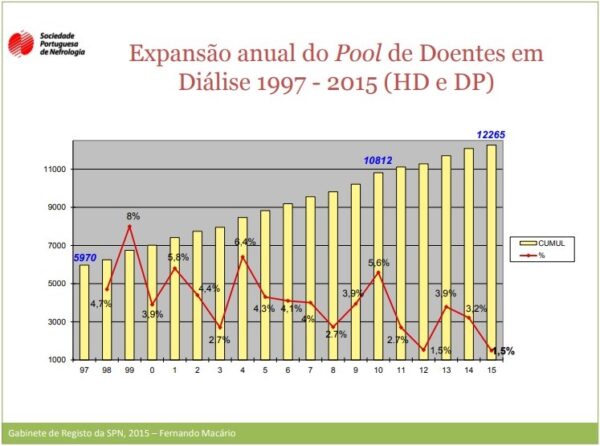
En Portugal, las estadísticas apuntan que alrededor de 800 mil personas sufren de enfermedad renal crónica y están siendo tratados 18.000 pacientes (dos tercios en diálisis y u tercio trasplantados), siendo la prevención primaria fundamental para reducir el número de personas que sufren de esta enfermedad1.
Figura 1 – Expansión anual del Pool de pacientes en Diálisis 1997 – 2015 [Informe del Gabinete de Registro de la Sociedad Portuguesa de Nefrologia, 2015]
La diálisis es un proceso catabólico que lleva a la desnutrición y que todos los estadios de la enfermedad renal crónica (ERC), o insuficiencia renal crónica (IRC) como es usualmente conocida, y de la DRT obligan a la evaluación, monitoreo e implementación de dietas específicas.
También el síndrome nefrótico (proteinuria superior a 3,5 g / día) obliga a restricciones y dietas específicas.
Así, la alimentación sana representa una ayuda obligatoria en la gestión de la enfermedad crónica renal e independientemente del estado de la función renal, esta debe ser parte esencial en la prevención y tratamiento, pudiendo:
- Garantizar necesidades nutricionales, evitando subnutrición o malnutrición.
- Ayudar a mantener el peso adecuado.
- Garantizar las necesidades energéticas de acuerdo con la actividad y el estado fisiológico.
- Disminuir peso sobre la función renal, evitando la degeneración.
- Reducir sintomatología como náuseas y / o disgeusia.
- Prevenir miolisis.
- Ayudar en el control de la glucosa y / o la diabetes y otros síndromes metabólicos.
Sugerimos:
- Sustitución de la leche por bebidas vegetales como avena o soja
- Linaza molida
- Glutation
- Probióticos
- Cordyceps sinensis
- Cupressus sempervirens L.
- Fragaria vesca
- Phyllanthus spp.
- Solidago virgaurea L.
Insuficiencia Renal Aguda
La insuficiencia renal aguda (IRA) tiene un inicio repentino y rápido deterioro de la función renal y una elevada tasa de mortalidad (alrededor del 60-65%), sin embargo, puede ser revertida, a diferencia de la DRC. Por supuesto que, a falta de un adecuado seguimiento médico y nutricional, su evolución hacia la enfermedad renal crónica es de alto riesgo y con esta, la necesidad de diálisis y / o trasplante.
Intervención Nutricional y Tratamiento
En ciertos pacientes puede ser necesario diálisis a corto plazo para evitar lesión renal y recuperar función basal, incluyendo en el tratamiento farmacológico diuréticos, resinas quelantes de potasio que actúan a nivel intestinal, insulina cuando ocurre hiperglicemia y bicarbonatos en los pacientes con acidosis. Dado que, generalmente, la IRA es un proceso catabólico, es necesaria una cuidadosa intervención nutricional, siendo las directrices comunes en práctica hospitalaria:
- Atenuar el catabolismo de la IRA para evitar la pérdida de proteínas viscerales y somáticas, siendo que la necesidad proteica variará según el estado renal, diálisis y estado proteico.
- En diálisis o si la función renal aumenta: 1,2 a 1,3g/kg de peso
- Sin diálisis: 0,6 – 0,8g/kg de peso
- Garantizar el aporte calórico que evite la pérdida de energía a través de proteínas
- Sensiblemente 35kcal/kg de peso
- Eventual limitación de electrolitos
- El sodio máximo [2 – 3]g/día para evitar la hipertensión y la retención de líquidos
- Monitorizar niveles de potasio y fósforo
- Monitorizar el balance de líquido
- En diálisis: la ingestión debe mantenerse entre los 1 y 1,5L / día
- Sin diálisis: Generalmente necesaria restricción para equiparar volumen de débito urinario +500ml
Dolencia Renal Crónica
En la enfermedad renal crónica (DRC) existe pérdida gradual y progresiva de la función renal, siendo ésta irreversible. Las causas más comunes son la diabetes y la hipertensión, las cuales causan cerca del 69% de los casos, pudiendo ser de origen infeccioso, por exposición a sustancias nefrotóxicas o enfermedades inmunes.
El paciente puede perder hasta un 75% de la función renal y mantenerse asintomático siendo necesario utilizar la tasa de filtración glomerular (TFG) para verificar el estado y la disfunción de la función renal y, por consiguiente, la fase de la DRC. Cuando la TFG alcanza valores inferiores a los 15 ml / min / 1,72m2 el enfermo entra en estadio 5 siendo clasificado como predializado o no dializado pues esta distinción hará variar la intervención nutricional la cual varía según estadio de la DRC y la necesidad de diálisis.
DRC No Dializados
A medida que la TFG disminuye los riñones pierden la capacidad de mantener los equilibrios ácido-base e hidroelectrolítico, debiendo el paciente ser seguido con exámenes complementarios de diagnóstico incluyendo hemoglobina, hematocrito, calcio, fósforo, perfil lipídico y, por supuesto, urea y creatinina plasmática , potasio, dióxido de carbono y cloruros.
En este estadio lo más importante es la preservación de la función renal por el mayor tiempo posible, posponiendo al máximo la entrada en estadio 5 y, con ello, la diálisis. Por lo tanto, es importante realizar un seguimiento / restricción proteica y de electrolitos (especialmente potasio).
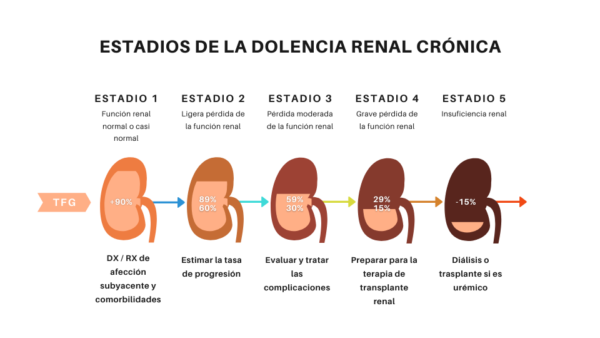 Figura 2 – Estadios de la Dolencia Renal Crónica
Figura 2 – Estadios de la Dolencia Renal Crónica
Intervención Nutricional y Tratamiento
En términos clínicos, las intervenciones se dirigen a las funciones renales principales que en estos pacientes se encuentran en rápido declive y se utilizan quelantes de fósforo, hierro intravenoso, agentes supresores de hormona paratiroidea (PTH), que se ajustan según los resultados de los exámenes de laboratorio de seguimiento.
Las directrices de Kidney Disease Outcomes Quality Initiative (KDOQI) establecen recomendaciones prácticas basadas en evidencia clínica según la fase de la DRC, recomendando evaluación y monitoreo nutricional a partir de fase 2 para evitar mayor daño sobre la función renal siendo de extraordinaria importancia el control de la glucemia e hipertensión. En cuanto a la intervención nutricional directa, ésta debe ayudar a controlar los síntomas urémicos como diarrea, vómitos y anorexia y prevenir la desnutrición. Las indicaciones específicas incluyen:
- Cálculo calórico y proteico basado en el peso corporal estandarizado (PCP) o ajustado (PCA) contemplando solamente necesidades de mantenimiento, debiendo el aporte calórico ser suficiente para atender a las necesidades calóricas y evitar el catabolismo proteico.
- Se debe dar especial relevancia al hecho de que el estrés y el nivel de actividad cambian las necesidades y se debe optar por proteínas de alto valor biológico (AVB) que deberán ser al menos el 50% del consumo proteico.
- En el caso de un paciente con diuréticos, el consumo de potasio no necesitará, al principio, de limitaciones, siendo estas implementadas conforme aumento por encima de los normales niveles séricos.
- Restricción de sodio por debajo de 1g.
- Control de ingesta de fósforo (a través del cual también es posible limitar la ingestión de calcio) para controlar niveles séricos de PTH, existiendo la necesidad de fármacos inhibidores de la absorción intestinal de fósforo.
- Limitar la ingesta de calcio a un máximo de 2g/día.
- Limitar la ingestión de líquidos, especialmente si existe una insuficiencia cardíaca congestiva y que los pacientes tratados con diuréticos deben ser especialmente monitorizados, ya que estos pueden causar progresión de la enfermedad renal debido a la depleción de volumen.
DRC Diálisis
Cuando el paciente alcanza estadio 5 surge la necesidad de diálisis la cual actúa como filtración artificial de la sangre, existiendo 2 tipos principales: hemodiálisis y diálisis peritoneal. En la hemodiálisis, la sangre proveniente de una arteria circula por un dializador mecánico en el que se filtra y es posteriormente devuelto a la circulación sanguínea a través de una vena paralela. En la diálisis peritoneal el peritoneo del propio paciente funciona como membrana de filtración entrando el dializado (solución hiperosmolar) por un catéter que atraviesa la pared abdominal y es infundido en la cavidad peritoneal. En ambas situaciones, la dieta es menos restrictiva en comparación con el estado de prediálisis.
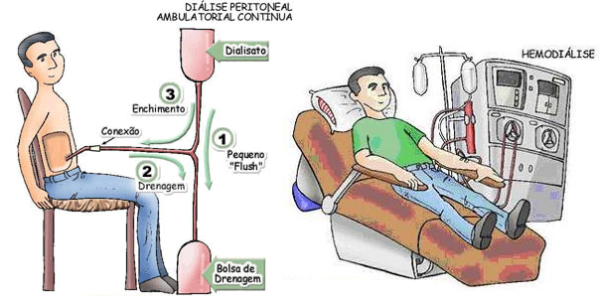
Figura 3 – Hemodiálisis y Diálisis Peritoneal
Intervención Nutricional y Tratamiento
Las necesidades calóricas y proteicas deben basarse en el PCP o PCA y proporcionar sólo cantidades necesarias para el mantenimiento. Una vez más, períodos de estrés y actividad física elevada deben aumentar las necesidades y, por lo tanto, la ingesta. Dado que el proceso de diálisis aumenta la pérdida de proteínas puede ser necesario aumentar el consumo (en comparación con la fase no dializada de la enfermedad). La preferencia debe recaer sobre las proteínas AVB en al menos el 50%.
Dado que la diálisis peritoneal utiliza glucosa en su dializado, en estos pacientes es especialmente importante controlar la glucemia e ingesta calórica, y el paciente diabético debe seguirse atentamente. Otras necesidades de controlo son:
- Potasio
- Diálisis peritoneal: ya que esta intervención puede aumentar la diuresis de este electrolito, estos pacientes pueden necesitar suplementación.
- Hemodiálisis: si existen pérdidas (usuales en las eventuales etiologías de la DRC como enfermedad renal poliquística y función renal residual significativa) o se utilizan diuréticos, puede ser necesaria la suplementación.
- Sodio
- La ingestión debe limitarse para controlar la sed y así mantener restringida la ingestión de líquidos, evitando edema.
- Fósforo
- Limitar la ingestión para reducir la estimulación de PTH, pudiendo ser necesaria la utilización de fármacos quelantes inhibidores de la absorción intestinal.
- Calcio
- La ingesta debe limitarse a dosis de 2000mg / día (dieta y eventual suplementación). Deberán monitorizarse atentamente los quelantes de fósforo a base de calcio, usuales en la industria alimentaria.
Para concluir, se debe garantizar el correcto apetito e ingesta alimentaria, siendo preferible que la dieta sea libre en vez de la colocación de demasiadas restricciones que lleven a la subnutrición.
En ciertos pacientes, en los que la ingestión es deficiente se pueden utilizar suplementos específicos como estimulantes del apetito y suplementos líquidos.
Gestión Nutricional de la Dolencia Crónica Renal2
A medida que la enfermedad renal crónica (CKD) avanza, aumenta la uremia, existe un desequilibrio electrolítico, y el equilibrio ácido-base y la retención de agua. En este cuadro, es usual verificar la enfermedad ósea siendo también común el desperdicio proteico-energético.
De esta forma, los autores de la última revisión acerca de la alimentación en la Enfermedad Renal Crónica publicada en noviembre de 2017, que resalta áreas importantes sobre la gestión nutricional, defienden que una dieta específica en estos pacientes puede mejorar la condición clínica, y recomiendan dosis nutricionales y dietarias de proteína , sodio, potasio, fósforo, calcio, fibras, calorías y grasas según el estadio de la enfermedad.
De acuerdo con esta revisión la excreción de bicarbonatos en sujetos sanos es de aproximadamente 30-34,6 ± 12,3 mmol / L, sin embargo los pacientes afectados excretan valores superiores, posiblemente debido a la oxidación incompleta de lípidos e hidratos de carbono que origina un aumento de la producción de ácido láctico y cetoácidos y que, por consiguiente, aumentan la carga iónica de hidrógeno de la producción diaria de ácido.
En pacientes con alto riesgo de enfermedad renal, sugieren un máximo de 1g / kg de peso, [0,6 – 0,8] g / kg de peso en pacientes con estadios avanzados de la enfermedad y / o proteinuria elevada, incluyendo aquí a los pacientes que iniciarán diálisis.
En diálisis, defienden que si el paciente realiza 3 o más sesiones por semana y presenta función renal residual, las dosis de proteína recomendadas deberán ser superiores a 1g / kg de peso, justificando que ésta es, de acuerdo con un estudio con la duración de 3 años y 30 075 participantes3, la que presenta menor tasa de mortalidad.
Por lo tanto, defienden que una dieta baja en proteínas puede disminuir la progresión de la enfermedad y ayudar a los pacientes a evitar o aumentar el tiempo sin necesidad de diálisis, sin que exista riesgo de cambios en el mecanismo de obtención de energía a través de proteínas o caquexia, al consumo de proteína vegetal, refiriéndose que esta está asociada al mejor estado general de salud, pudiendo disminuir la presión intraglomerular y proteinuria así como reducir la producción de urea.
En este aspecto se refiere incluso que las restricciones rigurosas al ingreso de potasio deben ser evitadas, ya que muchos de los alimentos ricos en potasio, como frutas y vegetales frescos, son ricos en fibra y vitaminas, presentan baja acidogénesis y son más saludables en términos cardiológicos así como menos aterogénicos que los alimentos bajos en potasio.
Concluye indicando que «dada la elevada incidencia y prevalencia de la enfermedad renal crónica y una urgente necesidad de estrategias alternativas en la gestión de la enfermedad, las intervenciones nutricionales con balizas específicas para cada patología que se dirijan al paciente y eficaces en términos de costes, pueden ayudar a la longevidad y disminuir la necesidad de diálisis».
Probióticos y Dolencia Renal
Diversos estudios defienden la importancia y demuestran el impacto que el microbioma representa sobre el estado de salud y bienestar, protegiendo contra agentes patógenos, educando a las células y contribuyendo a diversas funciones metabólicas, afectando directa o indirectamente diversas funciones fisiológicas4, demostrando que alteraciones en la composición y estructura de la microbiota humana, conocido por disbiosis, pueden predisponer a diversas patologías, explicando además susceptibilidades o resistencias a determinadas enfermedades5.
De hecho, estas alteraciones al microbioma están cada vez más relacionadas con el desarrollo de diversas enfermedades como obesidad6, dolencia oncológica7, diabetes8, enfermedad inflamatoria del intestino9, asma10, dolencia cardiovascular11 y dolencia renal12.
De hecho, la disbiosis en pacientes con CKD puede contribuir a un aumento de los niveles tóxicos de urea, que contribuye a la progresión de la enfermedad13.
Se debe tener en cuenta que las interacciones entre el microbioma y la enfermedad renal no son unidireccionales y, por lo tanto, la patología renal afecta a la estructura de la microbiota y contribuye a la disbiosis.
Dado que esta enfermedad está asociada a una disminución del consumo de fibras14 y al aumento de la frecuencia de la toma de antibióticos15, disminución del tránsito intestinal, congestión y edema de las paredes del intestino, hiperacidosis y suplementación con hierro16, y que estos factores están asociados la disbiosis y el aumento del número de agentes microbianos patógenos en el intestino, la suplementación con los probióticos correctos debe ser de extraordinaria importancia.
Muchos de estos factores mencionados anteriormente afectan a la permeabilidad intestinal que se ve aumentada ocurriendo translocación de productos bacterianos a través de las barreras intestinales y consecuentemente desencadenando respuestas inmunes que pueden explicar la inflamación sistémica que contribuye negativamente para el desarrollo de la enfermedad cardiovascular y renal17.
Otro posible mecanismo para la disbiosis en pacientes renales resulta del aumento de la secreción de urea gastrointestinal18 que siendo hidrolizada por los microorganismos origina elevada formación de amonio la cual afecta a las bacterias comensales y causa desequilibrio sobre la microbiota intestinal.
| Detalles | |
| Temática | Nutrición en la Patología Renal
|
| Alimentación | Dieta baja en proteína preferentemente de origen vegetal.
Monitorizar y limitar la ingestión de líquidos, potasio, calcio, fósforo y sodio. Sugerir aumento de ingestión de ajo, canela, Zingiber officinale, Camelia sinensis y Curcuma longa. |
| Fitoterapia / Nutriente | Bebidas vegetales de avena o soja.
Linaza molida Glutatión, Probióticos; Cordyceps sinensis; Cupressus sempervirens L.; Fragaria vesca; Phyllanthus spp.; Solidago virgaurea L. |
| Hábitos de vida | Ejercicio físico moderado, preferencia por hidrogimnasia; Higiene del sueño; Higiene alimentaria.
|
| Productos con acción beneficiosa | Renes Forte, Probiotic5, Advanced Pro, Turmeric Max Liposomado, Magnesium Citrate Liposomado, Omega 3 MaxPower.
|
| Link’s | UNC Kidney Health Library; An Integrative Approach to Advanced Kidney Disease in the Elderly; Guidelines for the use of alternative medicine for kidney patients
|
| Keyword’s | #Rim #Naturopatia #Nutrición #Dolencia_Renal_Crónica #Probióticos #Glutatión #Probióticos #Cordyceps_sinensis #Cupressus_sempervirens #Fragaria_vesca #Phyllanthus #Solidago_virgaurea
|
BIBLIOGRAFÍA & ESTUDIOS DE EVIDENCIA CIENTÍFICA
[1] Portal de Diálisis – Dia Mundial del Riñón 2017 in https://www.portaldadialise.com/articles/dia-mundial-do-rim-2017
The Clinical Dietitians’s Essential Pocket Guide, 1st Edition; Koogan, 2009;
[2] Nutritional Management of Chronic Kidney Disease. N Engl J Med. 2017 Nov 2;377(18):1765-1776.
[3] Is controlling phosphorus by decreasing dietary protein intake beneficial or harmful in persons with chronic kidney disease? Am J Clin Nutr. 2008 Dec;88(6):1511-8.
[4] How host-microbial interactions shape the nutrient environment of the mammalian intestine. Annu Rev Nutr. 2002;22:283-307.
Host-bacterial mutualism in the human intestine. Science. 2005 Mar 25;307(5717):1915-20.
[5] Dysbiosis of the gut microbiota in disease. Microb Ecol Health Dis. 2015 Feb 2;26:26191.
[6] Obesity and the gut microbiome: pathophysiological aspects. Horm Mol Biol Clin Investig. 2014 Jan;17(1):53-61.
[7] The microbiome and obesity-an established risk for certain types of cancer. Cancer J. 2014;20:176–180.
Microbiome, inflammation, and cancer. Cancer J. 2014;20:181–189.
[8] The intestinal microbiome in type 1 diabetes. Clin Exp Immunol. 2014;177:30–37.
Does the gut microbiome hold clues to obesity and diabetes? Curr Biol. 2013;23:R359–362.
[9] Irritable bowel syndrome, inflammatory bowel disease and the microbiome. Curr Opin Endocrinol Diabetes Obes. 2014;21:15–21.
The microbiome in inflammatory bowel disease: current status and the future ahead. Gastroenterology. 2014;146:1489–1499.
[10] Microbiota in allergy and asthma and the emerging relationship with the gut microbiome. Cell Host Microbe. 2015;17:592–602.
[11] Elevated levels of circulating DNA in cardiovascular disease patients: metagenomic profiling of microbiome in the circulation. PLoS One. 2014 Aug 18;9(8):e105221.
Contrasting circulating microbiome in cardiovascular disease patients and healthy individuals. Int J Cardiol. 2013;168:5118–5120.
[12] The intestinal microbiota, a leaky gut, and abnormal immunity in kidney disease. Kidney Int. 2013;83:1010–1016.
[13] Gut microbiome and kidney disease: a bidirectional relationship. Pediatr Nephrol. 2017 Jun;32(6):921-931.
[14] Food intake characteristics of hemodialysis patients as obtained by food frequency questionnaire. J Ren Nutr. 2002;12:17–31.
[15] Short-term antibiotic treatment has differing long-term impacts on the human throat and gut microbiome. PLoS One. 2010 Mar 24;5(3):e9836.
[16] Dietary management of chronic kidney disease patients: protein-restricted diets supplemented with keto/amino acids. Am J Nephrol. 2005;25 Suppl 1:1-28.
[Chronic kidney disease (CKD)–recent progress. Topics: VII. Management of chronic kidney disease (CKD) and treatment; 1. Dietary treatment and life-style management in CKD patients]. Nihon Naika Gakkai Zasshi. 2012 May 10;101(5):1340-6.
Dietary trends and management of hyperphosphatemia among patients with chronic kidney disease: an international survey of renal care professionals. J Ren Nutr. 2014 Mar;24(2):110-5.
[17] Gut microbiome in chronic kidney disease. Exp Physiol. 2016 Apr;101(4):471-7.
[18] The gastrointestinal tract in uremia. J Assoc Physicians India. 1997 Nov;45(11):833-4.